29.(6分)现有下列药品和实验仪器。
药品:石灰石、稀硫酸、稀盐酸
仪器如下:
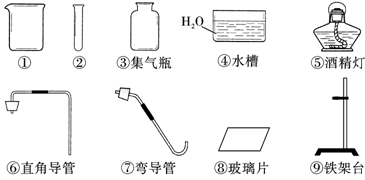
(1)写出未标注的仪器名称:① ,② 。
(2)实验室用题中药品制备并收集一瓶气体应选择的仪器是(填写仪器序号) ,反应的化学方程式为 。
30.(6分) A、B、C、D、E是初中化学中的五种常见物质。C、D是单质,C为紫红色固体,D被认为是最清洁的能源。B的浓溶液常用做干燥剂。已知Fe和A、B的水溶液分别能发生反应:
①Fe + A → C + E; ②Fe + B → D + E 。
(1)写出A、B、C的化学式: A , B ,C 。
(2)现有Fe和A、C三种固体组成的混合物,小刚想测定该混合物中C物质的质量分数,他设计并完成了以下实验:

你认为,小刚的实验数据处理是否正确(填“正确”或“ 不正确”) ,理由是 。
四、科学探究(共12分)请将答案填在答题卷上
31.请你参与下列探究:
【问题情景】在课外活动中,小斌按照课本实验(见图1)探究分子的运动时,闻到了刺激性的氨味,于是,小斌在老师的指导下,设计了如图2的实验装置,进行同样的实验,结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论。
【实验探究与结论】小斌用图2装置进行实验。
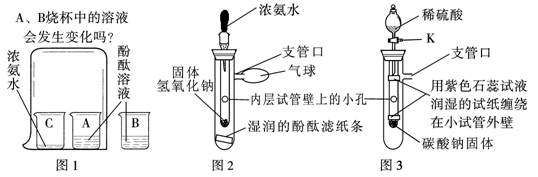
(1)滴入少量浓氨水后,湿润的酚酞滤纸条发生的变化是 。从分子运动的角度分析,此现象可说明的结论是 ;从浓氨水化学性质的角度分析,此现象可说明的结论是 。
(2)用初中的化学知识分析,固体氢氧化钠的作用是 。
(3)和课本实验比较,小斌改进后的装置的优点是(写出两点)① ;② 。
【思维拓展】小媚受小斌实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质。
(1)打开活塞K滴入稀硫酸后,两条用紫色石蕊试液润湿的试纸发生的相同变化是 ,不同变化是 ,小媚从课本实验中知道,二氧化碳和水本身都不能使石蕊变色,因而她认为以上两个变化验证的二氧化碳的性质依序是 、 。
(2)小柔认为小媚的装置还可以同时验证:①二氧化碳能使澄清石灰水变混浊 ;②二氧化碳不能燃烧,也不支持燃烧。
小柔为完成自己的两个验证实验,对小媚的实验进行的简单改进是: 、 。
五.细心推算(共10分)请将答案填在答题卡上
32.课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
请分析表中数据回答并计算[(4)要求写计算过程 ]
实验一实验二实验三实验四
原固体混合物质量10g10g10g10g
加入CaCl2溶液质量10g20g30g40g
生成的沉淀的质量2gm5g5g
(1)生成的沉淀是(填写化学式) 。
(2)10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为 g。
(3)m= g。
(4)原固体混合物中Na2CO3的质量分数是多少?
桂林市2010年初中毕业暨升学考试试卷化学试题参考答案及评分标准
一、选择题(每小题2分,共50分)
题号12345678910111213
答案ACDACDCDCDBCD
题号141516171819202122232425
答案ABABBADCBAAC
二.填空题(化学方程式每个2分,化学式错误、未配平均不给分;不写必要的反应条件、生成物状态漏标或错标合扣1分。其它每空1分。共16分)
26.(5分)(1)钠 (2)二氧化碳或CO2 小苏打(碳酸氢钠或NaHCO3)
(3)有机物 72:11:88 或 144:22:176
27.(6分)(1)Fe2O3 + 6HCl = 2FeCl3 + 3H2O
(2)C + 2CuO
(3)2KClO3
28.(5分)(1)B>A=C (或A=C
(2)C 降低温度 增加溶剂 (后两空不规定顺序)
三.简答题(化学方程式每个2分,化学式错误、未配平均不给分;不写必要的反应条件、生成物状态漏标或错标合扣1分。共12分)
29.[6分。(1)每空1分,(2)每空2分]
(1) ① 烧杯 ② 试管 (错别字不给分)
(2) ②③⑥⑧⑨ 或 ②③⑥⑧(不规定序号顺序)
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
30.[6分。(2)中最后一空2分,其余每空1分]
(1)CuSO4 H2SO4 Cu
(2)不正确 4.2g紫红色固体中包含有铁和硫酸铜反应生成的铜(铁和硫酸铜反应生成了铜 或 4.2g紫红色固体不只是原来的C物质 或 4.2g紫红色固体的质量大于原来C物质的质量。其它合理答案均可。没有文字说明不给分)
四.实验探究(共12分。每空1分)
31.【实验探究与结论】
(1)滤纸条变红(只答“变色”不给分)
分子在不断运动 或 浓氨水(氨 或 NH3 或 NH3·H2O)易挥发 浓氨水(NH3·H2O)显碱性 或 浓氨水(NH3·H2O)是碱性物质 或 氨气与水反应生成了碱或 浓氨水(NH3·H2O)易分解(合理答案均给分)
(2)氢氧化钠吸水放热,加速浓氨水的挥发 (只要答到“氢氧化钠吸水放热”就可给分)
(3)现象明显、快速出现实验现象、实验药品用量少、环保无污染 (答出其中的任意两点均给分)
【思维拓展】
(1)试纸由紫色变红色(答出“变红”即可,只答“变色”不给分)
下面的试纸先变红 或 两条试纸变色的快慢不同 或 两条试纸变色的深浅不同(若答“下面试纸变红,上面试纸不变红”不给分,其它合理答案均给分)
二氧化碳和水反应生成了酸(碳酸或酸性物质)
二氧化碳的密度比空气大 或 二氧化碳比空气重 (合理答案均给分。顺序错误不给分)
(2)在外管(或大试管)内加入澄清石灰水
将燃烧的木条放在支管口(以上两空不规定顺序,合理答案均给分)
五.计算题(共10分。计算过程没写必要的单位合扣1分,没写“答”但能表述清楚不扣分)
32.解:(1)CaCO3 (1分) (2)5 (2分) (3) 4 (2分)
(4)设10g原固体混合物中Na2CO3质量为x
CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
106 100
x 5g ………………………………………………… (1分)
x = 5.3g ………………………………………………… (1分)
固体混合物中Na2CO3的质量分数是53%………………… (2分 ,列式和结果各1分)
答:原混合物中碳酸钠的质量分数是53%。 (合理解答参照给分)